क्लोरीन क्या है इसका सूत्र, इलेक्ट्रॉनिक विन्यास, खोज, उपयोग और नुकसान

रसायन विज्ञान के एक और खास आर्टिकल क्लोरीन क्या है मै आपका बहुत स्वागत है। जिस प्रकार हमने अपने पिछले लेख में आपको सल्फर और नाइट्रोजन के बारे में विस्तार से बताया, उसी प्रकार आज हम आपको क्लोरीन गैस के बारे में संपूर्ण जानकारी देने जा रहे हैं। यह एक बहुत महत्वपूर्ण तत्व है जिसकी खोज आज से लगभग बहुत समय पहले हुई थी। आधुनिक आवर्त सारणी में क्लोरीन तत्व को 17 वें समूह में रखा गया है। तथा उस समूह के तत्वों को हैलोजन कहा जाता है।
आज के इस लेख के महत्वपूर्ण जैसे कि क्लोरीन की खोज किसने की क्लोरीन का सूत्र क्या है तथा क्लोरीन क्या है आदि के बारे में हर संभव चीज जानने का प्रयास करेंगे। बोर्ड परीक्षाओं में कई बार क्लोरीन बनाने की विधि के बारे में पूछ लिया जाता है। अतः हमने अपने लेख में इन सभी बातों को अच्छे से कवर किया है। विस्तृत जानकारी के लिए हमारे आर्टिकल को अंत तक अवश्य पढ़ें।
क्लोरीन क्या है?
यह एक रासायनिक तत्व है। जिसका परमाणु क्रमांक 17 होता है। क्लोरीन की खोज एक महान वैज्ञानिक शीले ने आज से लगभग 250 वर्ष पूर्व सन् 1774 ईस्वी में की थी। इन्होंने HCl अम्ल की क्रिया MnO2 से कराई। इस अभिक्रिया के फल स्वरुप क्लोरीन गैस प्राप्त हुई तथा साथ में मैग्नीज क्लोराइड और जल के अणु भी उत्पाद के रूप में प्राप्त हुए। 1810 वैज्ञानिक Davi ने इस गैस का नाम क्लोरीन (Chlorine) रख दिया।
क्लोरीन गैस द्वि अणुक होती है। Chlorine Ka Pratik अर्थात क्लोरीन का सूत्र Cl होता है। तथा क्लोरीन गैस का प्रतीक Cl2 होता है। हमने आपको निम्नलिखित बताया है कि क्लोरीन का सही इलेक्ट्रॉनिक विन्यास है
क्लोरीन का सूत्र = Cl & क्लोरीन गैस का सूत्र = Cl2
क्लोरीन के भौतिक गुण
- यह एक पीले रंग की तेज गंध वाली गैस होती है। अर्थात आप इसकी गंध से ही इस गैस को पहचान सकते हैं।
- यह जल में आसानी से घुल जाती है अर्थात यह जल में विलय होती है।
- भारानुसार यह वायु से लगभग ढाई गुना भारी होती है।
- क्लोरीन गैस अत्यधिक विषैली होती है।
- क्लोरीन गैस का घनत्व 3.214 ग्राम प्रति लीटर होता है।
- इस गैस का अणु भार 70.906 ग्राम प्रति मोल होता है।
क्लोरीन के कुछ रासायनिक गुण
- धातु तथा अधातु के साथ क्लोरीन अभिक्रिया करके धातु क्लोराइड का निर्माण करती है।
- क्लोरीन अपने विरंजक गुण के कारण एक प्रबल विरंजक की तरह कार्य करती है। अर्थात क्लोरीन जल अथवा नमी की उपस्थिति में पदार्थों का रंग उड़ा देती है और इसका यह गुण ऑक्सीकारक होता है।
- यह गैस हाइड्रोजन के साथ अभिक्रिया करके हाइड्रोक्लोरिक अम्ल का निर्माण करती है।
H2 + Cl2→ 2HCl
क्लोरीन बनाने की विधि
इस गैस को प्रयोगशाला में बनाने की विधि हम अपने इस आर्टिकल क्लोरीन क्या है मैं आपको विस्तार से बताएंगे। क्लोरीन के निर्माण की बहुत सारी विधियां हैं हम आपको उनमें से कुछ महत्वपूर्ण विधियों के बारे में बताएंगे जो की परीक्षा के लिए अति महत्वपूर्ण है।
1. प्रयोगशाला में क्लोरीन का निर्माण
प्रयोगशाला के अंदर सांद्र हाइड्रोक्लोरिक अम्ल की अभिक्रिया कुछ प्रबल ऑक्सीकारक पदार्थ हो जैसे कि KMnO4, MnO2, K2Cr2O7 आदि के साथ जब कराई जाती है तब क्लोरीन गैस (Cl2) प्राप्त होती है। इस अभिक्रिया को आप निम्नलिखित समीकरण से समझ सकते हैं।
MnO2 + 4HCl → MnCl2 + 4H2O + Cl2
2. औद्योगिक क्षेत्र में क्लोरीन का निर्माण
औद्योगिक विधियों में क्लोरीन के निर्माण की हम आपको यहां पर दो विधियां बताने जा रहे हैं जो कि निम्न प्रकार हैं –
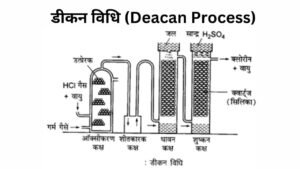
डीकन विधि (Deacan Process)
इस विधि के द्वारा क्लोरीन का औद्योगिक निर्माण किया जाता है और एक बड़े स्तर पर क्लोरीन गैस प्राप्त की जाती है। इस प्रकार की विधि में हाइड्रोजन क्लोराइड गैस को उत्प्रेरक क्यूप्रस क्लोराइड (CuCl2) की उपस्थिति में वायुमंडल की ऑक्सीजन के द्वारा ऑक्सीकरण कराते हैं जिससे फल स्वरूप क्लोरीन गैस प्राप्त होती है। इस विधि में 450 डिग्री सेंटीग्रेड ताप रखा जाता है। अभिक्रिया की समीकरण निम्नलिखित दी गई है।
4 HCl + O2 → 2 Cl2 + 2H2O
विधुत अपघटनी विधि (Electrolysis Method)
इसके द्वारा शुद्ध क्लोरीन का निर्माण किया जाता है और यह एक आधुनिक विधि है। विधुत अपघटनी विधि द्वारा क्लोरीन का निर्माण करने के लिए सोडियम क्लोराइड का जलीय विलयन तैयार किया जाता है। इस जलीय विलियन का विधुत अपघटन कराने पर एनोड पर क्लोरीन गैस प्राप्त होती है तथा कैथोड पर सोडियम प्राप्त होता है। इस विधि में जो सेल का प्रयोग किया जाता है उसे नेल्सन सेल कहा जाता है।
एनोड पर = 2 Cl− (aq) → Cl2 (g) + 2 e−

क्लोरीन गैस के उपयोग
इस गैस के कुछ प्रमुख उपयोग निम्न प्रकार है –
- इस गैस का प्रयोग कीटाणुओं को नष्ट करने के लिए किया जाता है।
- विभिन्न प्रकार की धातुओं के निष्कासन में भी इस का प्रयोग किया जाता है।
- कई प्रकार के विस्फोटक तथा रंजक के निर्माण के लिए क्लोरीन की सहायता ली जाती है।
- कपड़ा उद्योग तथा कपास उद्योग में विरंजक के रूप में क्लोरीन का बहुत बड़ा योगदान रहता है।
- विभिन्न प्रकार के रासायनिक यौगिकों जैसे कि ब्रोमीन, फास्फीन, विरंजक चूर्ण आदि के निर्माण में क्लोरीन का इस्तेमाल किया जाता है।
क्लोरीन गैस के नुकसान
इस गैस से कुछ नुकसान भी है जिन्हें आप को जानना बहुत जरूरी है अतः अपने इस लेख क्लोरीन क्या है के माध्यम से अब हम आपको क्लोरीन के नुकसान बताने जा रहे हैं जोकि निम्नलिखित हैं –
लंबे समय तक क्लोरीन के संपर्क में रहने से आपके स्वास्थ्य पर हानिकारक प्रभाव पड़ सकता है। क्लोरीन की तीखी गंध के कारण आपको स्वसन तंत्र आंखों और त्वचा से संबंधित समस्या की शिकायत हो सकती है। खांसी, आंखों में तथा त्वचा में जलन आदि हो सकती है। हालांकि पानी को साफ करने के लिए क्लोरीन का इस्तेमाल किया जाता है परंतु कहीं ना कहीं यह मानव जीवन पर बुरा असर डालता है जिसका परिणाम हमें कुछ समय के पश्चात अवश्य देखने को मिलता है।
निष्कर्ष
अभी तक हमने क्लोरीन के बारे में जितनी सारी बातें की आशा करता हूं कि आपको हमारी सारी बातें अच्छे ढंग से समझ में आई होंगी। हम प्रतिदिन आपके लिए रसायन विज्ञान से संबंधित नए नए लेख लेकर आते रहते हैं। हमारे आज के लेख क्लोरीन क्या है से संबंधित यदि आपका कोई सुझाव या प्रश्न बाकी रह गया हो तो आप अपनी बात हम तक कमेंट सेक्शन के माध्यम से पहुंचा सकते हैं। बहुत जल्द मिलेंगे एक नए लेख के साथ।




